 最新文章
最新文章
- 03-26 动物医学院与兆丰华集团...
- 03-26 长沙宠物行业市场交流会...
- 03-26 怀化职业技术学院来校调...
- 03-24 浏阳黑山羊脓包病防控技...
- 03-17 赣州浩东牧业有限公司来...
- 03-08 文利新教授团队学术理论...
 热门文章
热门文章
- 06-04 我校“十一五”国家级实...
- 06-24 知名学者王爱兵教授受聘...
- 06-26 我校杰出校友邓明义博士...
- 10-22 动医学院召开院领导见面会
- 11-04 神农学者” 特聘教授杨毅...
- 11-04 动医学院小动物医疗保护...
文利新教授团队首次揭示了慢性砷暴露诱发阿尔茨海默病样行为的新机制
砷是一种广泛存在于地下水中的环境污染物,全球仍有超亿人面临慢性砷暴露风险。近日,湖南农业大学动物医学院文利新教授团队首次揭示了慢性砷暴露通过调节肠-脑轴驱动阿尔茨海默病(AD)样行为的核心机制,其成果论文“Unveiling the gut-brain axis: How chronic exposure to arsenic-induced microglial pyroptosis drives Alzheimer's disease-like pathology”发表在国际权威Top期刊《Journal of Hazardous Materials》上(中科院1区,IF:11.3)。

长期接触砷可能诱发记忆力下降和认知障碍,甚至增加阿尔茨海默病(俗称“老年痴呆”)的发病风险。本研究模拟低(50 μg/L)、中(150 μg/L)、高污染区(450 μg/L)地下水中砷的含量,构建6个月慢性砷暴露小鼠模型,团队研究证实:慢性砷暴露可导致小鼠认知功能障碍、脑部出现β-淀粉样蛋白(Aβ)沉积和Tau蛋白过度磷酸化等典型AD样病理特征;团队进一步阐明了其机制:慢性砷暴露诱导肠道菌群紊乱和肠道屏障损伤,致使血清和脑组织中吲哚硫酸盐(IS)的异常蓄积。粪菌移植实验进一步证实,将慢性砷暴露小鼠的肠道菌群移植给正常小鼠,重现了认知功能障碍,AD样病例特征、IS蓄积及神经炎症表型,明确了肠道菌群紊乱在慢性砷致神经毒性中的核心作用。此外,研究还发现慢性砷暴露通过上调肝脏IS合成相关基因、下调肾脏IS排泄相关基因,形成“IS合成增加-排泄减少”的恶性循环,加剧其在脑内的蓄积与毒性,激活脑部AhR/NF-κB/NLRP3信号通路,诱发小胶质细胞焦亡。在小鼠小胶质细胞(BV2)模型中,团队发现砷与IS联合暴露可协同促进小胶质细胞M1型极化,削弱其对Aβ和Tau蛋白的吞噬功能,并通过AhR/NF-κB/NLRP3通路增强焦亡效应,证实AhR是砷-IS联合致神经毒性的关键调控靶点。
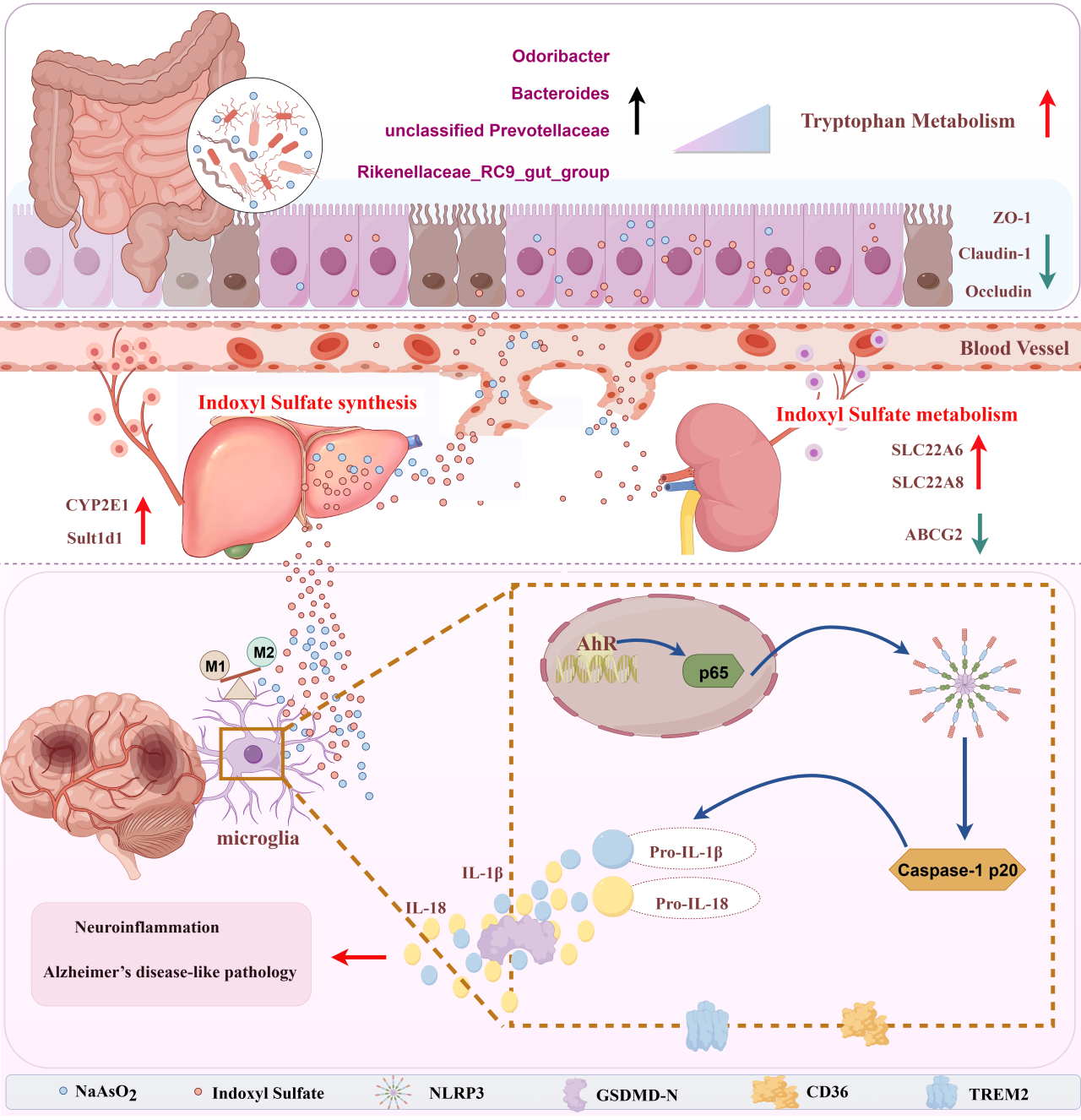
本成果首次揭示了“慢性砷暴露-肠道菌群紊乱-IS蓄积-AhR/NF-κB/NLRP3介导小胶质细胞焦亡-AD样行为”的级联机制,证实了肠-脑轴在环境毒物致神经退行性疾病中的枢纽作用,为环境砷污染相关神经退行性疾病的防治和产品创制提供了新的理论依据与干预靶点,对公共卫生砷污染防治具有重要指导意义。
本文共同第一作者为湖南农业大学屈建谕博士(生物科学技术学院和动物医学院联合培养)和姜鑫硕士,共同通讯作者为刘水平教授和文利新教授。该研究获得国家自然科学基金(32503127)、长沙市自然科学基金(kq2402116)、湖南省教育厅优秀青年项目(24B0204)和生猪产业前沿科学与关键技术研究课题(2019xny-js0440)的资助。
(初审:文利新,二审:李小英,终审:易金娥)
| 点击下载文件: |